
地址:北京市通州区观音庵南街1号院1号楼3层2单元304
电话:010-56231496 13366834635
邮箱:Byjy86@126.com
技术背景
基于mRNA-LNP技术的mRNA疫苗在人类对抗新冠等病毒的斗争中发挥了重要作用。针对病毒膜蛋白的mRNA疫苗在小鼠中可以产生强烈的免疫反应并有效产生病毒中和抗体1, 2。由于许多具有复杂结构的跨膜蛋白,都很难获得具有天然构象的抗原用于动物免疫,使得这类蛋白的抗体获得一直是科研界和产业界的技术难题。mRNA-LNP技术可以将体外合成的全长或部分mRNA递送到小鼠、兔子等动物体内,mRNA在细胞质中被翻译成所需的蛋白,定位到细胞膜上或被MHC呈递到APC细胞表面,激活免疫系统并产生针对天然构象的复杂结构膜蛋白的抗体,解决针对具有复杂结构蛋白的抗体开发问题。
本公司研发团队经过不断优化改进,成功建立了适用于复杂结构蛋白抗体开发的mRNA-LNP产品,可以实现构象完整的复杂结构膜蛋白在细胞表面高表达。通过这一技术可以用于抗体免疫和筛选,从而获取和筛选识别复杂结构靶点天然构象的功能性抗体。本公司除提供已有靶点的mRNA-LNP产品外,同时也接受定制服务。
技术原理
mRNA技术,是将体外合成的mRNA递送到体内中,mRNA在细胞质中被翻译成所需的蛋白质3。mRNA技术的快速发展已经实现了通过无细胞的体外转录方式获得高质量的标准化mRNA分子,并通过5 '端加帽、3 '端加PolyA和核苷修饰等技术增强mRNA的稳定性。由于mRNA是带负电荷的长链大分子,无法通过细胞膜脂质双分子层,因此需要使用脂质纳米颗粒(LNP)进行mRNA递送。
脂质纳米粒(LNP)是使用脂质形成的一种纳米微粒,作为一种多组分系统,LNP通常由可电离脂质、辅助磷脂、胆固醇和保护剂聚乙二醇化脂质组成。目前,LNP广泛用于核酸药物的体内递送4, 5。其优势在于:1)良好的生物相容性,促进细胞摄取;2)提高mRNA分子稳定性;3)提高内体逃逸。将LNP的四种组分(可电离脂质、DSPC、胆固醇、PEG-脂质)溶于乙醇中,与水溶液中的mRNA进行混合。可电离脂质通过与带负电的mRNA相结合,驱动囊泡的形成,使mRNA包裹在脂质纳米颗粒的内部,形成mRNA-LNP脂质纳米颗粒。
mRNA-LNP脂质纳米颗粒通过I.M.注射被免疫动物,包封在LNP内的mRNA在体内递送过程中受到保护,可避免RNA酶的降解,并通过膜融合作用被递送进细胞内。在细胞内,由于pH值的改变使得LNP与内体中的磷脂之间产生静电相互作用导致内体膜破裂,mRNA被释放到细胞质中,翻译为蛋白质。大多数细胞都可以成为mRNA-LNP脂质纳米颗粒的受体细胞,它们都有适当的内吞机制来内化,同时mRNA-LNP脂质纳米颗粒有效靶向特定的APC细胞(如树突状细胞DC)也是产生特异性应答的机制之一6。激活免疫系统并产生针对天然构象的复杂结构膜蛋白的抗体。

本公司产品独特优势
> 进一步优化5 '端加帽技术、3 '端加PolyA和核苷修饰技术增加mRNA稳定性
> 进一步优化5 '-UTR和3'-UTR序列增加mRNA的翻译效率
> mRNA可以在细胞膜表面表达目标抗原,且表达量显著提高,提高免疫原性
> 通过密码子优化进一步增加蛋白质折叠度、包封效率和翻译效率
> 蛋白具备全长结构、天然构象和生物学活性
> 可用于动物免疫、细胞表达(进一步用于抗体筛选和CAR阳性率检测)
案例展示
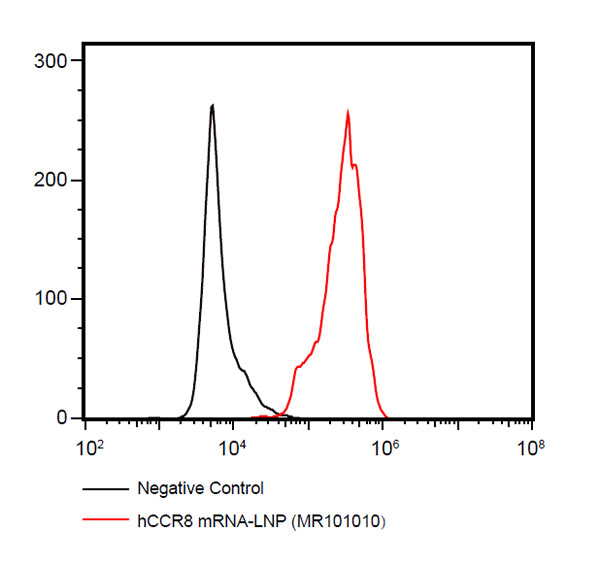
以GPCR蛋白CCR8为例,通过多项mRNA技术优化后外转录获得的mRNA与LNP组装成mRNA-LNP脂质纳米颗粒,转染293T细胞后利用流式细胞技术检测CCR8 mRNA表达情况。结果表明CCR8-LNP在细胞中具有良好的抗原表达水平。
参考文献
1. Laczkó, D. et al. A Single Immunization with Nucleoside-Modified mRNA Vaccines Elicits Strong Cellular and Humoral Immune Responses against SARS-CoV-2 in Mice - ScienceDirect. (2020).
2. Garrado, C.G., Curtis, A.D., Dennis, M., Pathak, S.H. & Permar, S.R. SARS-CoV-2 Vaccines Elicit Durable Immune Responses in Infant Rhesus Macaques. Science Immunology 6.
3. Sahin, U., Karikó, K. & Türeci, z. mRNA-based therapeutics — developing a new class of drugs. Nature Reviews Drug Discovery.
4. Wang, C., Zhang, Y. & Dong, Y. Lipid Nanoparticle–mRNA Formulations for Therapeutic Applications. (2021).
5. Samaridou, E., Heyes, J. & Lutwyche, P. Lipid nanoparticles for nucleic acid delivery: Current perspectives. Advanced Drug Delivery Reviews (2020).
6. Gilboa, E. & Vieweg, J. Cancer immunotherapy with mRNA-transfected dendritic cells. Immunological Reviews 199, 251-263 (2010).
- LNP及常用对照组
- 免疫检查点
- GPCR家族
- 溶质载体(SLC)家族
| 基因 | 货号 | 描述 | 应用 |
|---|---|---|---|
| GFP mRNA-LNP | MR100010 | GFP mRNA-LNP(MR100010)。 MR100010-SE为mRNA-LNP简化版产品,采用简化的技术流程,可满足常规的细胞转染和体内递送需求。 |
细胞转染 体内递送 |
| RFP mRNA-LNP | MR100020 | RFP mRNA-LNP(MR100020)。 MR100020-SE为mRNA-LNP简化版产品,采用简化的技术流程,可满足常规的细胞转染和体内递送需求。 |
|
| Luciferase mRNA-LNP | MR100030 | Luciferase mRNA-LNP(MR100030)。 MR100030-SE为mRNA-LNP简化版产品,采用简化的技术流程,可满足常规的细胞转染和体内递送需求。 |
|
| LNP | MR100040 | LNP(MR100040)。 MR100040-SE为mRNA-LNP简化版产品,采用简化的技术流程,可满足常规的细胞转染和体内递送需求。 |
| 基因 | 货号 | 描述 | 应用 |
|---|---|---|---|
| hCD161 mRNA-LNP | MR101530 | 人CD161全长mRNA-LNP(MR101530)。 MR101530-SE为mRNA-LNP简化版产品,采用简化的技术流程,可满足常规的细胞转染和体内递送需求。 |
细胞转染 体内递送 |
| hCD155 mRNA-LNP | MR101520 | 人CD155全长mRNA-LNP(MR101520)。 MR101520-SE为mRNA-LNP简化版产品,采用简化的技术流程,可满足常规的细胞转染和体内递送需求。 |
|
| hCD30L mRNA-LNP | MR101220 | 人CD30L全长mRNA-LNP(MR101220)。 MR101220-SE为mRNA-LNP简化版产品,采用简化的技术流程,可满足常规的细胞转染和体内递送需求。 |
|
| hPD-1 mRNA-LNP | MR101010 | 人PD-1全长mRNA-LNP(MR101010)。 MR101010-SE为mRNA-LNP简化版产品,采用简化的技术流程,可满足常规的细胞转染和体内递送需求。 |
|
| hPD-L1 mRNA-LNP | MR101020 | 人PD-L1全长mRNA-LNP(MR101020)。 MR101020-SE为mRNA-LNP简化版产品,采用简化的技术流程,可满足常规的细胞转染和体内递送需求。 |
|
| hCTLA-4 mRNA-LNP | MR101030 | 人CTLA-4全长mRNA-LNP(MR101030)。 MR101030-SE为mRNA-LNP简化版产品,采用简化的技术流程,可满足常规的细胞转染和体内递送需求。 |
|
| hTIM3 mRNA-LNP | MR101080 | 人TIM3全长mRNA-LNP(MR101080)。 MR101080-SE为mRNA-LNP简化版产品,采用简化的技术流程,可满足常规的细胞转染和体内递送需求。 |
|
| hLAG-3 mRNA-LNP | MR101090 | 人LAG-3全长mRNA-LNP(MR101090)。 MR101090-SE为mRNA-LNP简化版产品,采用简化的技术流程,可满足常规的细胞转染和体内递送需求。 |
|
| h4-1BB mRNA-LNP | MR101100 | 人4-1BB全长mRNA-LNP(MR101100)。 MR101100-SE为mRNA-LNP简化版产品,采用简化的技术流程,可满足常规的细胞转染和体内递送需求。 |
|
| hGITR mRNA-LNP | MR101110 | 人GITR全长mRNA-LNP(MR101110)。 MR101110-SE为mRNA-LNP简化版产品,采用简化的技术流程,可满足常规的细胞转染和体内递送需求。 |
|
| hOX40 mRNA-LNP | MR101120 | 人OX40全长mRNA-LNP(MR101120)。 MR101120-SE为mRNA-LNP简化版产品,采用简化的技术流程,可满足常规的细胞转染和体内递送需求。 |
| 基因 | 货号 | 描述 | 应用 |
|---|---|---|---|
| hGPR65 mRNA-LNP | MR101510 | 人GPR65全长mRNA-LNP(MR101510)。 MR101510-SE为mRNA-LNP简化版产品,采用简化的技术流程,可满足常规的细胞转染和体内递送需求。 |
细胞转染 体内递送 |
| hGCCR mRNA-LNP | MR101500 | 人GCCR全长mRNA-LNP(MR101500)。 MR101500-SE为mRNA-LNP简化版产品,采用简化的技术流程,可满足常规的细胞转染和体内递送需求。 |
|
| fasTM4SF5 mRNA-LNP | MR101480 | 猴TM4SF5全长mRNA-LNP(MR101480)。 MR101480-SE为mRNA-LNP简化版产品,采用简化的技术流程,可满足常规的细胞转染和体内递送需求。 |
|
| hTM4SF5 mRNA-LNP | MR101470 | 人TM4SF5全长mRNA-LNP(MR101470)。 MR101470-SE为mRNA-LNP简化版产品,采用简化的技术流程,可满足常规的细胞转染和体内递送需求。 |
|
| hCLDN 3 mRNA-LNP | MR101460 | 人CLDN3全长mRNA-LNP(MR101460)。 MR101460-SE为mRNA-LNP简化版产品,采用简化的技术流程,可满足常规的细胞转染和体内递送需求。 |
|
| hCX3CR1 mRNA-LNP | MR101450 | 人CX3CR1全长mRNA-LNP(MR101450)。 MR101450-SE为mRNA-LNP简化版产品,采用简化的技术流程,可满足常规的细胞转染和体内递送需求。 |
|
| hCXCR6 mRNA-LNP | MR101440 | 人CXCR6全长mRNA-LNP(MR101440)。 MR101440-SE为mRNA-LNP简化版产品,采用简化的技术流程,可满足常规的细胞转染和体内递送需求。 |
|
| hCXCR5 mRNA-LNP | MR101430 | 人CXCR5全长mRNA-LNP(MR101430)。 MR101430-SE为mRNA-LNP简化版产品,采用简化的技术流程,可满足常规的细胞转染和体内递送需求。 |
|
| hCXCR4 mRNA-LNP | MR101420 | 人CXCR4全长mRNA-LNP(MR101420)。 MR101420-SE为mRNA-LNP简化版产品,采用简化的技术流程,可满足常规的细胞转染和体内递送需求。 |
|
| hCXCR3 mRNA-LNP | MR101410 | 人CXCR3全长mRNA-LNP(MR101410)。 MR101410-SE为mRNA-LNP简化版产品,采用简化的技术流程,可满足常规的细胞转染和体内递送需求。 |
|
| hCXCR2 mRNA-LNP | MR101400 | 人CXCR2全长mRNA-LNP(MR101400)。 MR101400-SE为mRNA-LNP简化版产品,采用简化的技术流程,可满足常规的细胞转染和体内递送需求。 |
|
| hCXCR1 mRNA-LNP | MR101390 | 人CXCR1全长mRNA-LNP(MR101390)。 MR101390-SE为mRNA-LNP简化版产品,采用简化的技术流程,可满足常规的细胞转染和体内递送需求。 |
|
| hCCR10 mRNA-LNP | MR101370 | 人CCR10全长mRNA-LNP(MR101370)。 MR101370-SE为mRNA-LNP简化版产品,采用简化的技术流程,可满足常规的细胞转染和体内递送需求。 |
|
| hCCR9 mRNA-LNP | MR101360 | 人CCR9全长mRNA-LNP(MR101360)。 MR101360-SE为mRNA-LNP简化版产品,采用简化的技术流程,可满足常规的细胞转染和体内递送需求。 |
|
| hCCR8 mRNA-LNP | MR101350 | 人CCR8全长mRNA-LNP(MR101350)。 MR101350-SE为mRNA-LNP简化版产品,采用简化的技术流程,可满足常规的细胞转染和体内递送需求。 |
|
| hCCR7 mRNA-LNP | MR101340 | 人CCR7全长mRNA-LNP(MR101340)。 MR101340-SE为mRNA-LNP简化版产品,采用简化的技术流程,可满足常规的细胞转染和体内递送需求。 |
|
| hCCR6 mRNA-LNP | MR101330 | 人CCR6全长mRNA-LNP(MR101330)。 MR101330-SE为mRNA-LNP简化版产品,采用简化的技术流程,可满足常规的细胞转染和体内递送需求。 |
|
| hCCR5 mRNA-LNP | MR101320 | 人CCR5全长mRNA-LNP(MR101320)。 MR101320-SE为mRNA-LNP简化版产品,采用简化的技术流程,可满足常规的细胞转染和体内递送需求。 |
|
| hCCR4 mRNA-LNP | MR101310 | 人CCR4全长mRNA-LNP(MR101310)。 MR101310-SE为mRNA-LNP简化版产品,采用简化的技术流程,可满足常规的细胞转染和体内递送需求。 |
|
| hCCR3 mRNA-LNP | MR101300 | 人CCR3全长mRNA-LNP(MR101300)。 MR101300-SE为mRNA-LNP简化版产品,采用简化的技术流程,可满足常规的细胞转染和体内递送需求。 |
|
| hCCR2 mRNA-LNP | MR101290 | 人CCR2全长mRNA-LNP(MR101290)。 MR101290-SE为mRNA-LNP简化版产品,采用简化的技术流程,可满足常规的细胞转染和体内递送需求。 |
|
| hCCR1 mRNA-LNP | MR101280 | 人CCR1全长mRNA-LNP(MR101280)。 MR101280-SE为mRNA-LNP简化版产品,采用简化的技术流程,可满足常规的细胞转染和体内递送需求。 |
|
| hXCR1 mRNA-LNP | MR101380 | 人XCR1全长mRNA-LNP(MR101380)。 MR101380-SE为mRNA-LNP简化版产品,采用简化的技术流程,可满足常规的细胞转染和体内递送需求。 |
|
| hGPR84 mRNA-LNP | MR101260 | 人GPR84全长mRNA-LNP(MR101260)。 MR101260-SE为mRNA-LNP简化版产品,采用简化的技术流程,可满足常规的细胞转染和体内递送需求。 |
|
| hCMKLR1 mRNA-LNP | MR101270 | 人CMKLR1全长mRNA-LNP(MR101270)。 MR101270-SE为mRNA-LNP简化版产品,采用简化的技术流程,可满足常规的细胞转染和体内递送需求。 |
|
| hCLDN6 mRNA-LNP | MR101250 | 人CLDN6全长mRNA-LNP(MR101250)。 MR101250-SE为mRNA-LNP简化版产品,采用简化的技术流程,可满足常规的细胞转染和体内递送需求。 |
|
| hGPR171 mRNA-LNP | MR101230 | 人GPR171全长mRNA-LNP(MR101230)。 MR101230-SE为mRNA-LNP简化版产品,采用简化的技术流程,可满足常规的细胞转染和体内递送需求。 |
|
| hHCAR1 mRNA-LNP | MR101240 | 人HCAR1全长mRNA-LNP(MR101240)。 MR101240-SE为mRNA-LNP简化版产品,采用简化的技术流程,可满足常规的细胞转染和体内递送需求。 |
|
| hCB1 mRNA-LNP | MR101210 | 人CB1全长mRNA-LNP(MR101210)。 MR101210-SE为mRNA-LNP简化版产品,采用简化的技术流程,可满足常规的细胞转染和体内递送需求。 |
|
| hCCR4 mRNA-LNP | MR101040 | 人CCR4全长mRNA-LNP(MR101040)。 MR101040-SE为mRNA-LNP简化版产品,采用简化的技术流程,可满足常规的细胞转染和体内递送需求。 |
|
| hCCR8 mRNA-LNP | MR101050 | 人CCR8全长mRNA-LNP(MR101050)。 MR101050-SE为mRNA-LNP简化版产品,采用简化的技术流程,可满足常规的细胞转染和体内递送需求。 |
|
| hGPR20 mRNA-LNP | MR101060 | 人GPR20全长mRNA-LNP(MR101060)。 MR101060-SE为mRNA-LNP简化版产品,采用简化的技术流程,可满足常规的细胞转染和体内递送需求。 |
|
| hLGR5 mRNA-LNP | MR101070 | 人LGR5全长mRNA-LNP(MR101070)。 MR101070-SE为mRNA-LNP简化版产品,采用简化的技术流程,可满足常规的细胞转染和体内递送需求。 |
|
| hCXCR2 mRNA-LNP | MR101130 | 人CXCR2全长mRNA-LNP(MR101130)。 MR101130-SE为mRNA-LNP简化版产品,采用简化的技术流程,可满足常规的细胞转染和体内递送需求。 |
|
| hCXCR4 mRNA-LNP | MR101140 | 人CXCR4全长mRNA-LNP(MR101140)。 MR101140-SE为mRNA-LNP简化版产品,采用简化的技术流程,可满足常规的细胞转染和体内递送需求。 |
|
| hCXCR5 mRNA-LNP | MR101150 | 人CXCR5全长mRNA-LNP(MR101150)。 MR101150-SE为mRNA-LNP简化版产品,采用简化的技术流程,可满足常规的细胞转染和体内递送需求。 |
| 基因 | 货号 | 描述 | 应用 |
|---|---|---|---|
| hSLC2A4 mRNA-LNP | MR101490 | 人SLC2A4全长mRNA-LNP(MR101490)。 MR101490-SE为mRNA-LNP简化版产品,采用简化的技术流程,可满足常规的细胞转染和体内递送需求。 |
细胞转染 体内递送 |
| hLIV-1 mRNA-LNP | MR101160 | 人LIV-1全长mRNA-LNP(MR101190)。 MR101190-SE为mRNA-LNP简化版产品,采用简化的技术流程,可满足常规的细胞转染和体内递送需求。 |
|
| hSLC7A11 mRNA-LNP | MR101170 | 人SLC7A11全长mRNA-LNP(MR101170)。 MR101170-SE为mRNA-LNP简化版产品,采用简化的技术流程,可满足常规的细胞转染和体内递送需求。 |
|
| hSLC3A2 mRNA-LNP | MR101180 | 人SLC3A2全长mRNA-LNP(MR101180)。 MR101180-SE为mRNA-LNP简化版产品,采用简化的技术流程,可满足常规的细胞转染和体内递送需求。 |
|
| hSLC16A1 mRNA-LNP | MR101190 | 人SLC16A1全长mRNA-LNP(MR101160)。 MR101160-SE为mRNA-LNP简化版产品,采用简化的技术流程,可满足常规的细胞转染和体内递送需求。 |
|
| hSLC43A2 mRNA-LNP | MR101200 | 人SLC43A2全长mRNA-LNP(MR101200)。 MR101200-SE为mRNA-LNP简化版产品,采用简化的技术流程,可满足常规的细胞转染和体内递送需求。 |


